PRESENTACIÓN
"Todo es veneno y nada es veneno, sólo la dosis hace el veneno" (Paracelso)
La historia del tratamiento de las enfermedades autoinmunes y la del tratamiento del cáncer, han corrido, en cierta medida, de forma paralela. Una consecuencia nefasta de la Primera Guerra Mundial fueron las devastadores lesiones de los combatientes expuestos al gas mostaza. Pero, una vez más, se hizo verdad (aunque fuera a consta de terribles sufrimientos) la máxima “no hay mal que por bien no venga”. La gravísima y mortal leucopenia que se observó en los expuestos a este agente llevó a intentar el empleo de sus derivados (mostazas nitrogenadas) en pacientes con linfomas en grado muy avanzado. Los resultados iniciales de esta terapéutica, desalentadores en principio, abrieron un nuevo camino y una gran esperanza en los pacientes con cáncer: la quimioterapia, mediante ciclofosfamida (emparentada con aquel terrorífico gas) y otros citostáticos, para destruir las células cancerosas. Pronto se comprobó que estos mismos fármacos, en dosis más reducidas, poseían un importante efecto inmunosupresor, lo que llevo a su utilización en el tratamiento de las enfermedades autoinmunes. No termina aquí el paralelismo. En las últimas décadas se han realizado importantísimos descubrimiento acerca de los mecanismos moleculares implicados en la respuesta inmune (tanto en el terreno de la autoinmunidad como en el del cáncer). Es sobre este tema, el de la inmunoterapia en el cáncer, de lo que trata la colaboración del doctor José Andrés Moreno Nogueira que traemos hoy a nuestra Tribuna.
Licenciado (con Premio Extraordinario) y Doctor en Medicina por la Universidad de Sevilla, el doctor Moreno se sintió atraído desde muy joven por la Oncología desde su especialidad en Medicina Interna y su amplia experiencia adquirida en la Clínica Universitaria de Navarra, la Fundación Jiménez Díaz, el Instituto de Tumori de Milán (Italia) y su participación constante en las Reuniones de la American Society of Clinical Oncology (ASCO), en Estados Unidos, durante más de 15 años. Fue fundador y Presidente de la Sociedad Española de Oncología Médica (SEOM) y Presidente del Comité Técnico de la Asociación Española contra el Cáncer. Presidente de la 1ª Comisión Nacional de Oncología Médica, tuvo un papel fundamental en la creación de esa especialidad y en el diseño de los programas de formación MIR. Jefe del Servicio de Oncología Médica del Hospital Universitario Virgen del Rocío, de Sevilla (donde tuve la suerte de contar con sus consejos y enseñanzas durante mi formación como internista), Profesor asociado de Oncología en la Facultad de Medicina de Sevilla y de Patología Médica en la Escuela Universitaria de Enfermería en su Hospital, es considerado el padre de distintas generaciones de oncólogos que se han formado y han aprendido gracias al trabajo y las investigaciones (más de un centenar de proyectos de investigación) desarrollados en el ámbito científico y asistencial dirigido por el doctor Moreno Nogueira. Académico numerario de la Real Academia de Medicina de Sevilla, se ha hecho acreedor de numerosas distinciones como la Medalla de Oro de Sevilla, el Premio Honorífico 2019 de la Sociedad Andaluza de Oncología Médica, el Premio "Galeno" del Real Colegio de Médicos de Sevilla o el Premio Fundación ECO en la Real Academia Nacional de Medicina de Madrid. El doctor Moreno es, además, un prolífico autor de obras relacionadas con su especialidad. En la sección de “Publicaciones” de nuestra web encontrarán enlaces para la descarga, libre, de varias de ellas. Un motivo más para estarle sumamente agradecido.
Julio Sánchez Román
Secretario de AADEA
ARTÍCULO
Cuando se analiza la historia de la inmunoterapia y su relación con el cáncer, se encuentra que los fundamentos de este tratamiento, desde sus épocas más iniciales, consisten en incrementar las defensas del organismo contra el cáncer. De tal manera que las investigaciones sobre la respuesta inmunológica han sido prioritarias en las últimas décadas. Investigaciones que han conducido al desarrollo de nuevas estrategias terapéuticas, tema central de este artículo, y que han significado un cambio en el paradigma del tratamiento del cáncer.
Los primeros pasos en relación a la inmunoterapia en el cáncer hay que remontarlos a 1800, cuando los médicos alemanes W. Busch y Friedrich Fehleisen notaron la regresión de tumores en pacientes con cáncer después de infecciones accidentales como la erisipela.
En 1868, W. Busch inoculó intencionalmente erisipela a un paciente con cáncer y notó una reducción del tumor. Posteriormente F. Fehleisen repitió este tratamiento en 1882 con el Streptococcus pyogenes en tumores de varios pacientes, observando cierto grado de respuestas.

La forma de activar el sistema inmunológico del paciente se inició realmente a finales del siglo XIX gracias a los experimentos del cirujano y oncólogo William B. Coley (1862-1936) basado en todo lo anterior, especialmente en los investigadores W. Busch y F. Fehleisen. En la revisión de la literatura, que hizo de toda la época, halló unos 47 casos sobre el efecto “favorable” de las infecciones en los tumores. Como no existían datos de investigación fiables, “decidió” probar su teoría en pacientes gravemente afectados y sin esperanza de vida. Así, en 1891, inyectó bacterias de erisipela del tipo Streptococcus pyogenes en el tumor de un paciente gravemente afectado por un sarcoma y a quien se le había pronosticado una evolución de solo unas pocas semanas de vida. Lo trató con una cepa muy agresiva de la bacteria introduciéndola directamente en el tumor, lo que hizo que el paciente empeorase. Sin embargo, a las 24 horas, el tumor empezó a disminuir, pronto se resolvió, y el paciente se pudo recuperar. Dado el peligro que implicaba la utilización de estreptocócicos vivos, Coley continuó sus tratamientos utilizando organismos muertos por calor, combinados con Serratia marcescens y endotoxinas activas, mezcla que se conoció como “la toxina de Coley” (M. Villanueva - Meyer, Rev. Galenus 098). Estas aportaciones de W. Coley fueron el punto de partida de una larga línea de investigaciones en inmunoterapia, que han llegado hasta la fecha, sin olvidarnos del tratamiento del cáncer superficial de vejiga, tras la resección transuretral, seguido de la aplicación de la vacuna de BCG, que ha demostrado ser un tratamiento adyuvante eficaz en el control de estos tumores, siendo aprobado por la FDA en 1990.
La nueva etapa de investigación sobre la inmunoterapia en cáncer sienta sus las bases en el desarrollo de los “inhibidores de puntos de control inmunológico”, que han mejorado indudablemente los resultados terapéuticos en diversos tipos de neoplasias, existiendo ya diferentes fármacos tanto en desarrollo clínico como en la práctica diaria.
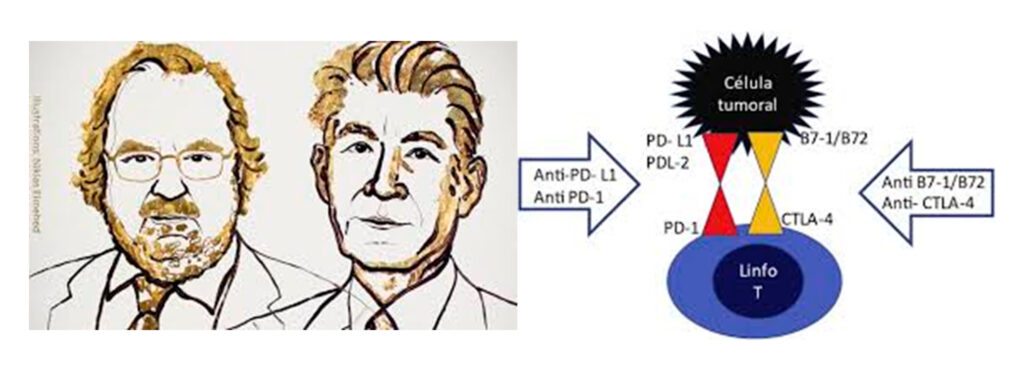
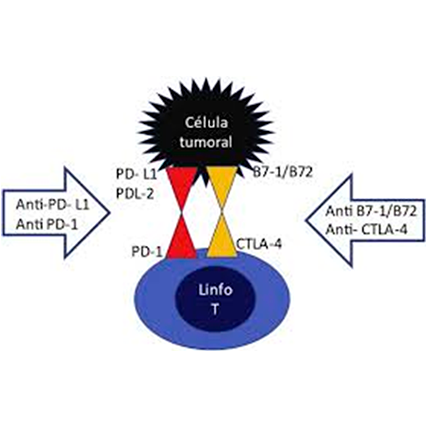
Los receptores en los linfocitos T, CTLA-4 y PD-1, descubiertos por J. Alisson y T. Honjo, respectivamente (Premio Nobel de Medicina 2018), cuando son estimulados, inducen una inactivación de dichos linfocitos. Se ha demostrado que la inhibición de estas vías de control permite activar a los linfocitos T para erradicar de forma eficaz a las células neoplásicas. En 1987 se clonó por primera vez la molécula coinhibitoria CTLA-4 (Cytotoxic T-Lymphocyte Antigen 4). Como consecuencia de este papel inhibitorio de CTLA-4 en la activación de los linfocitos T, lógicamente se pensó que su bloqueo podría mejorar su respuesta antitumoral. Dicha inhibición del crecimiento tumoral podría hacerse mediante anticuerpos monoclonales, lo que se experimentó en modelos murinos de fibrosarcoma, carcinoma de colon, próstata, mama, ovario, melanoma, linfoma etc. La FDA aprobó el anticuerpo monoclonal anti–CTLA-4 denominado ipilimumab en el tratamiento de pacientes con melanoma metastásico en los que se obtuvieron respuestas antitumorales importantes.
Ensayos clínicos posteriores demostraron beneficios claros de supervivencia en general en el 30% de los pacientes, obteniéndose respuestas de larga duración: aproximadamente el 22% de los pacientes se mantuvieron libres de enfermedad por 10 años.
La regulación positiva de la vía PD-1 ocurre más tarde en la respuesta inmune, siendo PD-1 más relevante en las células T después de la exposición persistente al antígeno, como en el caso de infecciones crónicas o tumores. De manera similar a CTLA-4, las células tumorales pueden usar esta vía de inhibición del receptor DP-1 para "apagar" la actividad antitumoral de las células T para evitar, así, su propia destrucción; y todo ello porque estas células tumorales han evolucionado al expresar el ligando de DP-1, DP-L1, que se une con PD-1 en las células T e inicia el proceso inhibidor. Al bloquear PD-1 o PD-L1, las células tumorales ya no pueden iniciar la inhibición de las células T, y el sistema inmunológico las puede identificar de manera más adecuada para su destrucción. En definitiva las células tumorales desarrollan PD-L1 para unirse con PD-1 en las células T, lo que evita que estas destruyan a las células tumorales.

Las importantes aportaciones de los investigadores Arlene Sharpe y Gordon Freeman, pertenecientes a la Harvard Medical School, lograron identificar los dos ligandos de PD-1: PD-L1 y PD-L2, confirmando el papel inmunosupresor de esta vía de señalización, y descubrieron además la expresión de PD-L1 y PD-L2 en células tumorales, proponiendo así a PD-1 y PD-L1/L2 como mecanismos de escape tumoral.
El tratamiento de pacientes con “inhibidores de puntos de control inmunitarios” (anti-CTLA-4, anti-PD-1, anti-PD-L1: terapia combinada anti-PD-1/PD-L1 con anti-CTLA-4) ha supuesto, sin duda, un gran avance en el campo del tratamiento del cáncer en los últimos años, con una mejora significativa en el resultado del tratamiento y en el pronóstico de los pacientes con diferentes tipos de neoplasias malignas; pero también el oncólogo tendrá que enfrentarse a nuevos efectos secundarios y saber cómo manejarlos.
En definitiva se ha abierto un fututo de incalculable valor para el manejo y tratamiento de los pacientes con cáncer, estando también en pleno desarrollo las vacunas contra el cáncer.
“La vida no es sino una continua sucesión de oportunidades para sobrevivir”.
(Gabriel García Márquez).

Dr. José Andrés Moreno Nogueira